
- Låg burn-rate om ca 5 MSEK per år (5 MSEK under 2017 och 5.4 MSEK under 2016)
- Tryggad kassa på ca 20 MSEK
- Mycket goda prekliniska resultat
- Till skillnad från befintliga läkemedel kan Toleranzias huvudläkemedelskandidat bota eller ge långvarig terapeutisk effekt
- Fas I/IIa-studie inleds 2019:
Mejl från VD Charlotte Fribert
”Fördelen jämfört med sedvanlig fas I-studie är att förutom kunskap om just säkerhet och tolererbarhet kan man redan i en första studie få initial information om läkemedlets effekt i patienter.”
- Utlicensiering efter fas I/IIa innebär att bolaget endast kommer ha kliniska kostnader fram till och med fas I/IIa, därefter kommer kassaflödet vara positivt i form av milestones och intäkter från royalties
- Toleranzia har beviljats särläkemedelsstatus för TOL2 i USA, innebärande bland annat särskild marknadsexklusivitet om 7 år efter marknadslansering och särskilt stöd från myndigheter
- Sannolikt utfall för marknadslansering är 25.3 %. Siffran ska jämföras med 9.6 % sannolikhet generellt för läkemedel

- Kortare tidsram från fas III till marknad jämfört med sedvanliga läkemedel
- Marknadspotentialen för TOL2 uppgår till 1,2 miljarder USD
- Färdig plattformsteknologi med stor flexibilitet som kan användas för att utveckla läkemedelskandidater för flera olika autoimmuna sjukdomar och bredda portföljen utan några markanta kostnader
- Toleranzia har redan identifierat och påbörjat preklinisk utveckling av en ny läkemedelskandidat inom ytterligare en autoimmun sjukdom, där det medicinska behovet är mycket stort. Denna kandidat kommer bolaget fortsätta att utveckla när TOL2 går in i kliniska studier.
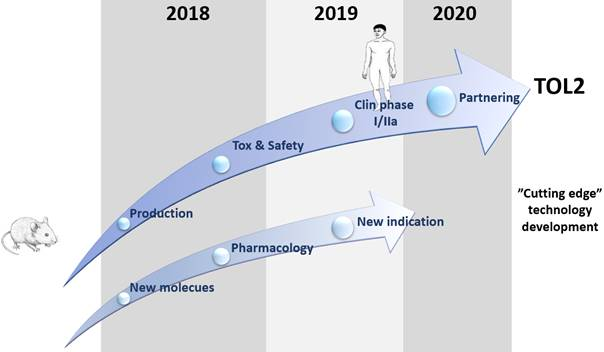
- Nuläge och vägen framåt
- 2018
Storskalig tillverkning har redan påbörjats
Toxikologi- och säkerhetsstudier – har redan inletts - 2019
Toxikologi- och säkerhetsstudier – avslutning
Klinisk fas I/IIa-studie – inledning - 2020
Klinisk fas I/IIa-studie – avslutning
Partnerskap med ett större läkemedelsbolag avseende TOL2
- 2018
TOLERANZIA
I denna bolagsanalys presenteras Toleranzia AB. Bolaget är det senaste tillskottet i portföljen och tillkom i samband med den nyligen genomförda nyemissionen.
Toleranzia, som grundades av forskare vid universitetet i Göteborg, har erhållit Orphan Drug Designation i USA och EU för sin plattformsteknologi som möjliggör utveckling av terapier som riktar sig mot sjukdomsorsaken – inte bara mot dess symptom. Forskningsframsteg ledde till att bolagets huvudläkemedelskandidat i mars 2017 beviljades särläkemedelsstatus i USA. Bolaget upprätthåller dessutom sin patentportfölj för plattformsteknologin, som i dagsläget rymmer godkända patent i USA, Japan, Kina, Australien och åtta länder i Europa, samt patentansökningar i ytterligare ett antal länder. Tillsammans med rapporterade positiva prekliniska resultat för bolagets tolerogen och stärkt patentskydd för teknologiplattformen pekar detta på en stark utveckling.
Inom läkemedelsforskningen har det länge funnits en önskan att kunna framkalla tolerans i immunsystemet som en väg mot att behandla autoimmuna sjukdomar. Toleranzia har utvecklat en metod för induktion av immunologisk tolerans hos patienter, och driver ett huvudprojekt inriktat specifikt mot den autoimmuna nerv- och muskelsjukdomen myastenia gravis. Med de prekliniska data som uppnåtts menar bolaget att myastenia gravis-tolerogenet har potential att bli den första verkligt sjukdomsmodifierande behandlingen för patienter med myastenia gravis. Till skillnad från befintliga alternativ har Toleranzias behandling potential att kunna bota eller ge långvarig terapeutisk effekt. Toleranzias läkemedelskandidat botar sjukdomen genom att återställa tolerans i immunsystemet. Därav namnet Toleranzia.
Att Toleranzias läkemedelskandidat har visat potential att påverka själva sjukdomsorsaken, medför en högre marknadspotential där man som ”first mover” normalt sett kan få fördelar som följer av att vara först ut med en ny behandlingsterapi. Utöver myastenia gravis har Toleranzias plattformsteknologi utvärderats mot ytterligare tre indikationer – reumatoid artrit, multipel skleros och diabetes typ 1, där positiva behandlingseffekter enligt bolaget har uppnåtts i sjukdomsrelevanta djurmodeller.
Toleranzias toleransinducerande terapi är sjukdomsspecifik och påverkar endast den del av immunsystemet som är kopplad till den enskilda sjukdomen, medan övriga delar av immunförsvaret som är centrala för vår hälsa lämnas intakta, såsom förmågan att skydda mot infektionssjukdomar och förmågan att hindra cancerutveckling.
Särläkemedel och särläkemedelsstatus
Läkemedel som utvecklas för orphan-sjukdomar klassificeras som särläkemedel och kan erhålla särläkemedelsstatus. Analysen återkommer till särläkemedel och särläkemedelsstatus i en separat del. Men låt oss redan här beakta följande. Särläkemedel har en mycket högre sannolikhet än övriga läkemedel att från fas I nå marknaden: 25.3 %. Detta ska jämföras med 9.6 % för alla läkemedel. Detta är i särklass den högsta siffran sett till samtliga läkemedel. Mer än 25 procent av samtliga särläkemedelskandidater går alltså hela vägen från fas I-studier till marknadslansering. Siffran tål att upprepas: mer än var fjärde särläkemedelskandidat går hela vägen fram till marknadslansering.

Bolagets unika plattformsteknologi, framgångsrika prekliniska studier tillsammans med att Toleranzia är ett särläkemedelsbolag är centrala faktorer som jag tror utgör grunden för en resa som kommer göra bolaget till en väldigt gynnsam investeringskandidat.
TOLERANZIAS PLATTFORMSTEKNOLOGI
Tolerogener
Autoimmuna sjukdomar utgör en grupp på ca 100 olika sjukdomar, som orsakas av att kroppens immunsystem felaktigt angriper och förstör kroppsegna ämnen och vävnader. Som nämnts ovan finns idag inget botemedel för denna grupp sjukdomar. Därför finns ett mycket stort medicinskt behov av nya och bättre behandlingsmetoder, som kan återskapa patientens tolerans mot de kroppsegna beståndsdelar som angrips vid den autoimmuna sjukdomen.
Toleranzia utvecklar läkemedelskandidater som utnyttjar immunförsvarets egen kraft och har därför möjlighet att möta det stora medicinska behovet av nya och bättre behandlingar för autoimmuna sjukdomar.
Kort om bolagets plattformsstrategi
Toleranzia jobbar med ett plattformstänk. Toleranzias plattformsteknologi innefattar framtagning av unika biologiska läkemedel som kallas tolerogener. Dessa baseras på sjukdomsspecifika, kroppsegna proteiner.
Första steget blir att visa att konceptet fungerar för en indikation (sjukdomstillstånd). Efter det ska man gå vidare och ta sig an andra indikationer bland de autoimmuna sjukdomarna. Lyckas Toleranzia med MG är plattformen validerad och erfarenheterna betydande.
För att bevisa nyttan med sin plattformsteknologi ska Toleranzias första läkemedelskandidat TOL2 behandla nerv- och muskelsjukdomen myastenia gravis (MG). MG har valts som den första indikationen för att det är en sjukdom som framför allt riktar sig mot ett protein i kroppen vilket innebär att dess sammansättning är känd. Utvalda delar av de kroppsegna proteinerna utgör själva läkemedlet. Som ett resultat av behandlingen kommer de sjukdomsspecifika proteinerna åter att uppfattas som kroppsegna ämnen och deras funktion i kroppen normaliseras.
Toleranzias unika plattformsteknologi ger bolaget möjlighet att framställa läkemedel som botar autoimmuna sjukdomar – utan negativ inverkan på immunförsvarets normala funktioner
Om Toleranzias plattformsteknologi
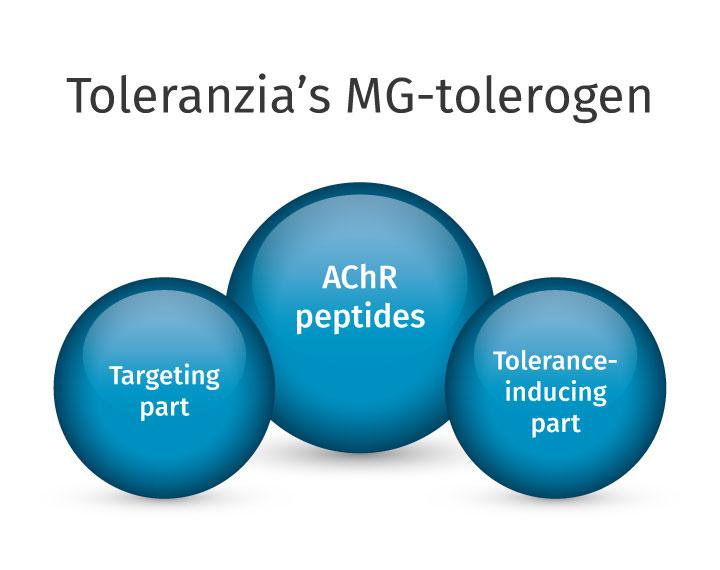
Toleranzias teknologi med tolerogener bygger på en proteinbaserad molekyl bestående av tre olika delar;
- En målsökande del.
- En toleransinducerande del.
- En sjukdomsspecifik del.
Den första delen styr molekylen så att den når rätt celler i kroppen vari den andra delen inducerar tolerans mot det sjukdomsspecifika ämne som utgör den tredje delen.
Exemplet Myastenia Gravis
Kännetecknande för sjukdomen är uttröttbarhet och muskelsvaghet som orsakas av en försämrad överföring av nervimpulser till muskulaturen. Detta beror på en immunattack riktad mot acetylcholinreceptorn (AchR) som är muskelns relästation och mottagare av signaler från nerven. När immunsystemet förstör AchR leder detta till en defekt neuromuskulär överföring av elektriska impulser och en efterföljande muskelsvaghet, som kan bli mycket allvarlig för patienten.
Toleranzias toleransinducerande terapi (plattformsteknologi) är, som tidigare nämnts, sjukdomsspecifik och påverkar endast den del av immunsystemet som felaktigt förstör våra fungerande celler. I fallet MG är det AchR som Toleranzias läkemedel (TOL2) korrigerar, medan övriga delar av vårt immunförsvar, som är centralt för vår hälsa, lämnas intakta. Som ett resultat av behandlingen kommer AchR åter att uppfattas som ett kroppseget ämne och dess roll i överföringen av signaler mellan nerv och muskel normaliseras.
Toleranzias plattformsteknologi är applicerbar på, och kan skräddarsys för, andra autoimmuna sjukdomar
Toleranzias tolerogener är mycket flexibla och bygger på att man först identifierar proteindelar som är specifika för en viss sjukdom. Därefter konstruerar man ett helt nytt biologiskt läkemedel som består av de sjukdomsspecifika kroppsegna proteindelarna. De sjukdomsspecifika proteinerna kan anpassas för en rad olika autoimmuna sjukdomar.
Toleranzias plattformsteknologi lägger alltså grunden till att utveckla unika läkemedel för varje specifik sjukdom. Förenklat kan man beskriva det som att Toleranzias teknologi först möjliggör en identifiering av det protein i kroppen som (felaktigt) angrips av kroppens immunförsvar. Därefter möjliggör plattformsteknologin att man kan framställa ett specifikt läkemedel som ser till att kroppens immunförsvar förstår vad det egentligen ska göra, dvs. inte angripa den friska delen som immunförsvaret ger sig på. Således uppfattas de angripna proteinerna åter som kroppsegna ämnen (att de ska finnas i våra kroppar) och deras funktion i kroppen normaliseras. Om plattformsteknologin fungerar för utvecklingen av ett läkemedel kommer den också att fungera för utvecklingen av andra läkemedel.
Toleranzias plattformsteknologi bygger på peptider och det finns flera autoimmuna sjukdomar där problempeptiden är känd. Det innebär att det blir möjligt att skräddarsy plattformen för andra autoimmuna sjukdomar.
Utöver Toleranzias primära indikation, myastenia gravis, har Toleranzias teknologiportfölj redan utvärderats mot ytterligare tre indikationer – positiva behandlingseffekter har uppnåtts i för människa relevanta djurmodeller av diabetes typ 1, reumatoid artrit och multipel skleros. Detta validerar Toleranzias teknologi som en teknologiportfölj med bred applikationspotential för utveckling av nya terapier inom autoimmuna sjukdomar.
Fördelar som bolagets unika plattformsteknologi medför
- Toleranzias plattformsteknologi kan användas som grund för utvecklingen av läkemedel för flera andra indikatorer. Detta medför också ett klart mervärde för investerare. Bolaget är inte beroende av en läkemedelskandidat. Istället har man en unik, patenterad plattformsteknologi som erhållit Orphan Drug Designation i USA och EU. Med plattformsteknologin som grund kan bolaget (och framtida samarbetspartners) utveckla flera andra läkemedel.
- Toleranzias plattformsteknologi oskadliggör endast den del av immunsystemet som felaktigt angriper kroppsegna ämnen medan övriga delar av vårt immunförsvar, såsom den livsviktiga förmågan att bekämpa infektionssjukdomar och att hindra cancerutveckling, lämnas helt intakta. Nuvarande terapier är inte sjukdomsspecifika utan påverkar alla delar av vårt immunförsvar vilket medför risk för allvarliga infektioner och andra negativa biverkningar.
- Denna unika teknik i sig ger Toleranzia en väldigt stor potential att utvecklas till ett bolag med en läkemedelsportfölj som gör bolaget unikt på marknaden. Därutöver gör den bolaget till en attraktiv uppköpskandidat/partner för läkemedelsjättarna (Big Pharma) med resurser och distributionskanaler att satsa på utvecklingen av flera läkemedelskandidater, baserat på Toleranzias unika plattformsteknologi. Detta förtjänar att betonas och jag återkommer till detta i analysen. Vi kan redan här konstatera att Toleranzia är ett oerhört attraktivt bolag för investerare.
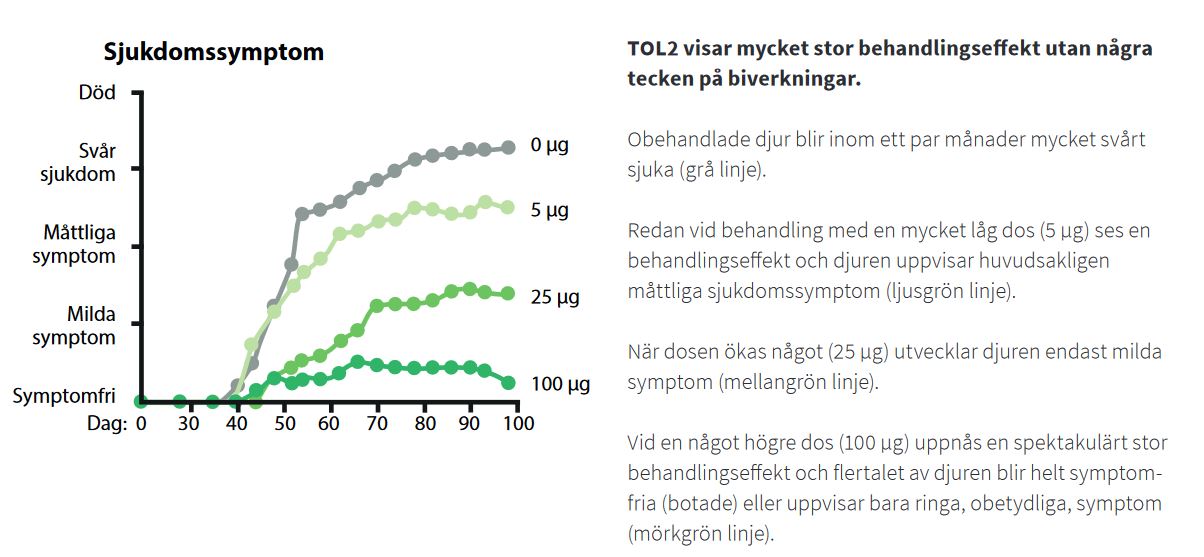
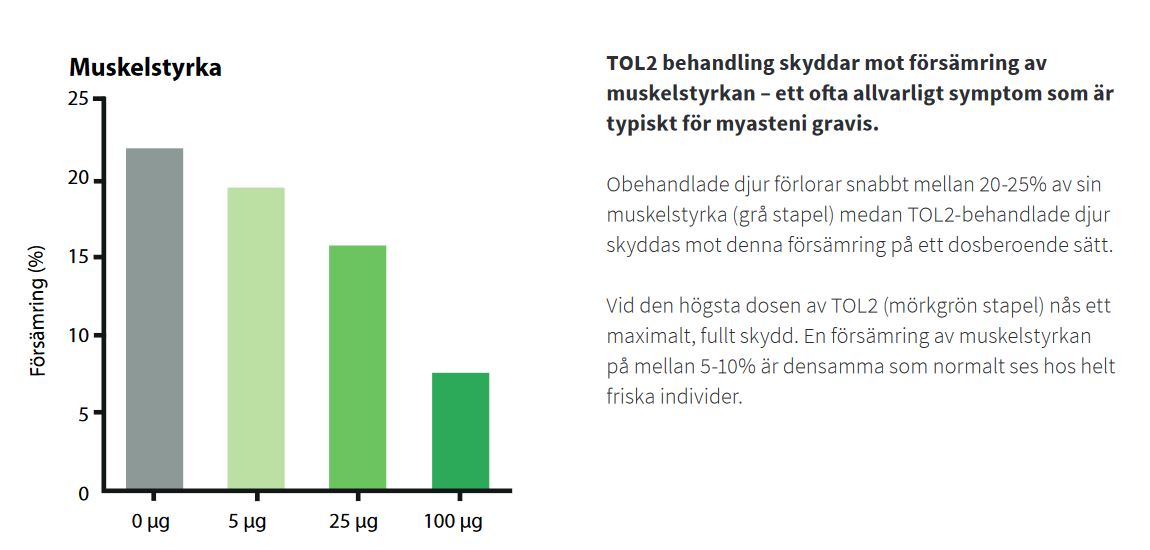
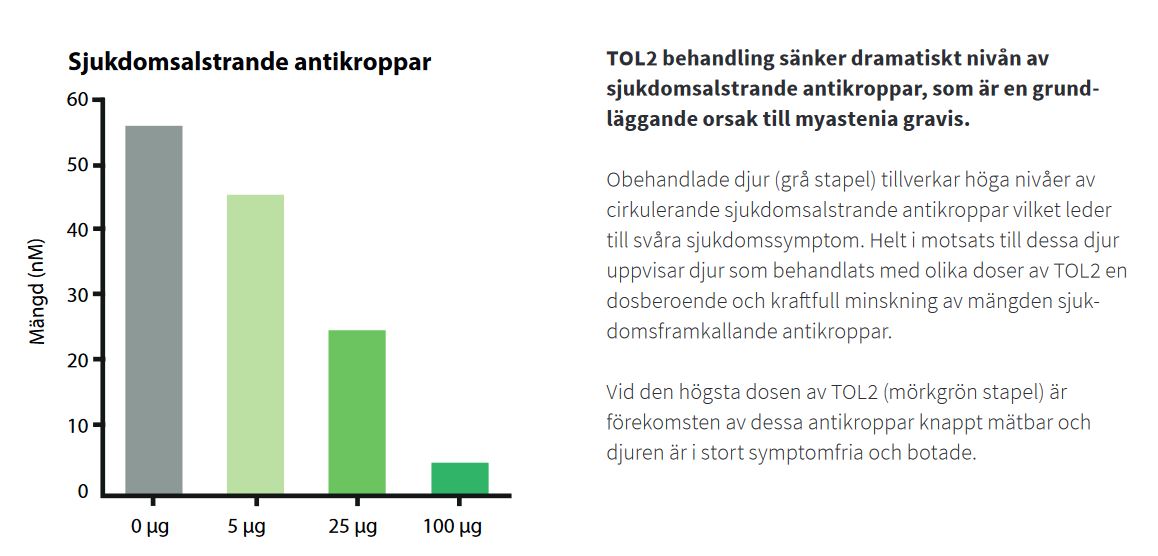
Prekliniska studier med mycket goda resultat för TOL2 och en enkel tillverkningsprocess av läkemedlen
Tillsammans med en forskargrupp vid Hellenic Pasteur Institute i Aten har Toleranzia genomfört prekliniska studier med TOL2 i en djurmodell av myastenia gravis. Den uppvisade mycket goda egenskaper. Behandlingseffekten var stor utan tecken på biverkningar och TOL2 har botande effekt på sjukdomen.
Resultaten från de prekliniska studierna för TOL2

Vägen framåt
Storskalig tillverkning av TOL2, toxicitets- och säkerhetsstudier och klinisk fas I/IIa-studie
- 2018
Storskalig tillverkning har redan påbörjats
Toxikologi- och säkerhetsstudier – har redan inletts - 2019
Toxikologi- och säkerhetsstudier – avslutning
Klinisk fas I/IIa-studie – inledning - 2020
Klinisk fas I/IIa-studie – avslutning
Partnerskap med ett större läkemedelsbolag avseende TOL2
Toleranzia inledde nyligen storskalig tillverkning av TOL2 tillsammans med den franska kontraktstillverkaren PX Therapeutics. Avtalet innebär att PX’ först kommer att tillverka TOL2 för de återstående prekliniska studierna avseende toxicitets- och säkerhetsstudier (d.v.s. studier av giftighet och tolererbarhet hos patienter vid olika dosnivåer). De kommer därefter producera material enligt GMP (good manufacturing practice) för den kommande kliniska fas I/IIa-studien, som Toleranzia beräknar inleda på patienter med myastenia gravis under 2019. Produktion enligt GMP innebär att produktionen håller de kvalitetskrav som myndigheter har för kommersialisering av produkten. En fas I/IIa-studie skiljer sig från fas I-studie på det sättet att studien, som avser säkerhet och tolererbarhet, genomförs direkt i patienter – alltså inte i friska frivilliga som är fallet i en klassisk fas I studie. En stor fördel med detta är att förutom kunskap om just säkerhet och tolererbarhet kan man redan i en första studie få initial information om läkemedlets effekt i patienter.
Toleranzia har sedan tidigare en utvecklad tillverkningsprocess för TOL2 i laboratorieskala och inom ramen för det nya avtalet kommer PX’ att skala upp tillverkningen så att tillräckliga kvantiteter av material som uppfyller den europeiska läkemedelsmyndighetens (EMA) krav kan tas fram för att inleda toxstudier under Q3 2018. PX’ är en väletablerad kontraktstillverkare med expertis och omfattande erfarenhet av den tillverkningsmetod som används för TOL2, samt resurser att möta Toleranzias krav på tidslinjer.
Toleranzias VD Charlotte Fribert kommenterar
“Vi är väldigt glada att ha ingått ett avtal med PX’ vilket gör att vi nu, mycket snabbt, efter valet av ny läkemedelskandidat, kommer igång med industriell produktion av TOL2 för våra kommande prekliniska och kliniska studier.”
Exit – kommersiella samarbetsavtal/utlicensiering
Om Toleranzia i kommande fas I/IIa-studie kan visa att TOL2 är ett säkert och effektivt läkemedel för myastenia gravis, har bolaget mycket goda möjligheter att träffa kommersiellt mycket attraktiva överenskommelser med ledande läkemedelsföretag. Toleranzias affärsmöjligheter säkerställs genom att Toleranzia kontinuerligt marknadsför sina projekt och samarbetsmöjligheter via etablerade kanaler och nya externa kontakter.
Parallellt har bolaget identifierat och påbörjat preklinisk utveckling av en ny läkemedelskandidat inom ytterligare en autoimmun sjukdom där det medicinska behovet fortfarande är mycket stort.
Källor
https://www.svd.se/toleranzia-battre-sent-an-aldrig#sida-2
http://www.toleranzia.se/wp-content/uploads/Toleranzia_IM_2018-02-13-FINAL.pdf
Toleranzias affärsmodell – tidig klinisk forskning och därefter ingå kommersiellt samarbetsavtal/utlicensieringsavtal
Toleranzias mål är att slutföra det prekliniska arbetet med TOL2 och genomföra en fas I/IIa-studie i myastenia gravis-patienter varefter bolaget avser att ingå ett kommersiellt samarbetsavtal med ett ledande läkemedelsbolag för finansiering av den senare kliniska utvecklingen och lanseringen av produkten. Parallellt med detta bedriver bolaget även akademiska och kommersiella samarbeten och utvärderar kontinuerligt nya spjutspetsteknologier inom autoimmuna sjukdomar, som ett sätt att maximera värdet i projekten.
Bolagets interna verksamhetsfokus ligger på preklinisk och tidig klinisk forskning och utveckling, parallellt med affärsutveckling för att hitta lämplig partner för kommersialisering. Fortsatt klinisk utveckling och kommersialisering kommer att ske i partnerskap med ledande läkemedelsföretag.
Bolagets mål är att om tre år framgångsrikt ha genomfört en klinisk fas I/IIa-studie och utlicensiering av TOL2, samt att ha identifierat och påbörjat preklinisk utveckling av en ny läkemedelskandidat inom ytterligare en autoimmun sjukdom.
Tilltalande affärsmodell ur ett investerarperspektiv
- Exit
Ur ett investerarperspektiv är det viktigt att förstå den biten att projektet säljs efter Fas I/IIa alternativt ingår partnerskap för att på ett betydligt vis minska kostnaderna för fortsatta studier. Risken i en investering minskar radikalt om man siktar på att bara investera över Fas I/IIa. Således kommer bolaget endast ha kliniska kostnader fram till och med Fas I/IIa och därefter kommer kassaflödena vara positiva i form av milestones och intäkter från royalties.
Den riskreducerande korta investeringshorisonten, och en tydlig och uttalad strategi som kan ta bolaget mot en “exit” i någon form är tilltalande ur ett investerarperspektiv.
- Enastående sannolikhet att nå marknad
Med de resultat som TOL2 visar och dess särläkemedelsstatus samt den marknadsandel på en miljardmarknad som ett framtida läkemedel riktas mot så ska bolaget uppvärderas rejält. Med 25 % sannolikhet för samtliga läkemedel som erhållit särläkemedelsstatus (vilket TOL2 har) att ta sig från Fas 1 till marknad, så kommer en lyckad Fas 1 att ge Toleranzia en betydligt högre sannolikhet än så att nå marknad. Någon siffra vill jag inte spekulera i, men att säga att den ligger långt över 50 % är inte att på något sätt sticka ut hakan.
- Låg burn-rate
Därtill ska bolagets låga burn-rate nämnas. Bolaget har i dagsläget en kassa om ca 26 MSEK. Toleranzia är exemplarisk att hålla hårt i kassan. Bolaget avverkade endast 5,4 MSEK under 2017 och 5 MSEK under 2016. VD Charlotte Fribert styr bolaget exemplariskt och kan konsten att hålla nere kostnaderna samtidigt som bolaget drivs framåt.
Marknadspotential – 1,2 miljarder USD
Låt oss också titta närmare på marknadspotentialen.
Toleranzia gör bedömningen att priset på behandlingen skulle kunna uppgå till cirka 40 000 USD per patient och år. Medianpriset för en behandling per patient och år var cirka 84 000 USD år 2016 för ”Top 100” särläkemedel i USA. Om en verkligt sjukdomsmodifierande behandling skulle lanseras på marknaden bör peak-sales för den europeiska och amerikanska marknaden kunna uppgå till minst 1,2 miljarder USD.
Noterbart är att denna marknadsestimering endast avser indikationen myastenia gravis och att 10–12 procent av patienterna nås av behandlingen. Den totala myastenia gravis-marknaden och den totala marknaden – som utgörs av omkring 100 olika autoimmuna sjukdomar – är förstås betydligt mer omfattande. Förutsatt framgångsrika kliniska studier har bolagets behandling potential att gynna flertalet patienter med myastenia gravis och i framtiden även många fler patienter med andra autoimmuna sjukdomar.
Kommersialiseringen planeras att utföras i partnerskap med ett läkemedelsföretag. Det är Bolagets bedömning att den amerikanska och den europeiska marknaden, oavsett partner, är av huvudintresse som läkemedelsmarknader.
http://www.toleranzia.se/wp-content/uploads/Toleranzia_IM_2018-02-13-FINAL.pdf
Konkurrenter
Idag finns ingen av bolaget känd behandling som slår mot sjukdomens grundläggande orsak, patienter med myastenia gravis behandlas med symptomlindrande terapier. Alla nuvarande behandlingar har gemensamt att de har en begränsad effektivitet och att de inte är sjukdomsspecifika utan även negativt påverkar sådana delar av immunsystemet som vi behöver för vårt normala immunförsvar. Detta resulterar i högre infektionskänslighet och risk att utveckla cancer för patienter som genomgår dessa behandlingar. Därför finns det ett mycket stort behov av nya och effektiva behandlingsalternativ att erbjuda patienter med myastenia gravis. Toleranzias läkemedelskandidat skiljer sig mot konkurrenternas genom att slå mot grundorsaken och inte bara symptomen och att den utgör en unik, riktad terapi som verkar endast mot den delen av immunsystemet som faktiskt orsakar sjukdomen. Toleranzias läkemedelskandidat har därför potential att på ett mer effektivt sätt långtidsverkande behandla eller helt bota myastenia gravis.
Patent och immateriella rättigheter
Toleranzia har ett teknologipatent som ger ett brett skydd avseende delar av Bolagets toleransteknologi. Ingivningsdatum för patentet är 2010-10-28 i Sverige och då löptiden är 20 år gäller det till och med 2030-10-28 i Sverige.
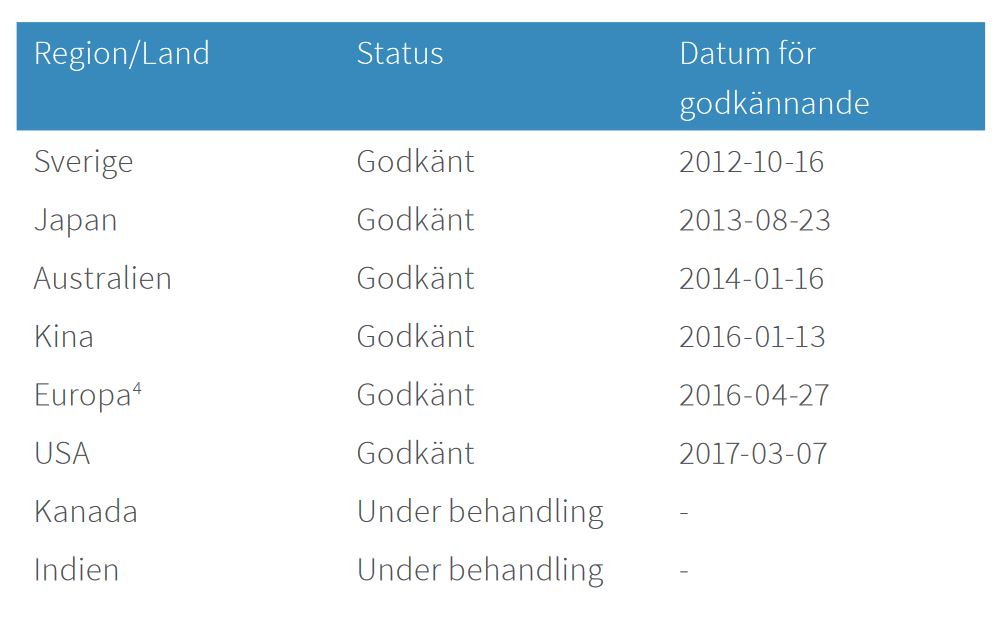
Utöver ovanstående teknologipatent har Toleranzia även kommersiellt skydd i form av särläkemedelsstatus.
Utöver dessa skydd utgör unik know-how en viktig del av Toleranzias immateriella tillgångar. Varje enskilt skydd är viktigt för en eventuell köpare eller partner och en kombination av alla ovan nämnda skydd stärker naturligtvis Bolagets möjlighet till kommersiellt attraktiva affärer.
Börsplus och Analyst Group
Börsplus och Analyst Group har båda släppt analyser av Toleranzia så sent som i mars 2018.
Analyst Group
Analyst Group gör en gedigen genomlysning av Toleranzia i sin analys. Här återges enbart analytikerns riktkurser.
- Base scenario: 7,4 kr
- Bull scenario: 29,7 kr
- Bear scenario: 0,7 kr.

Börsplus
Börsplus har följt Toleranzia under flera år och har således släppt flera analyser av bolaget. Här sammanfattas den senaste analysen från den 15 februari 2018.
”Bioteknikbolaget Toleranzia är efter förseningar på banan igen med läkemedelskandidat TOL2 mot den autoimmuna sjukdomen myastenia gravis. Värderingen i den pågående nyemissionen är låg och riskvilliga bioteknikinvesterare kan ta sig en närmare titt på bolaget.”
”I vår första analys av Toleranzia beräknade vi nuvärdet av projektvärdet för MG till strax under 300 Mkr (nuvarande börsvärde är omkring 45 MSEK). Det finns ingen anledning att ändra på det och visar att det finns stor potential i aktien om Toleranzia tar sig genom framgångsrika kliniska studier. Plattformen är då validerad och har ett betydande värde.”



[…] Toleranzia har varit tydliga och systematiska med att målet är att ingå ett kommersiellt samarbetsavtal med ledande läkemedelsbolag. Dels för finansieringen av den senare kliniska utvecklingen, dels för lanseringen av läkemedelskandidaten TOL2. Bolaget har också kommunicerat detta mål till marknaden vid flera tillfällen (läs mer här). […]